-
-
-
Tổng tiền thanh toán:
-

Amino axit tác dụng với H2SO4 - phương pháp giải và các dạng bài tập
17/05/2021 Đăng bởi: Công ty cổ phần CCGroup toàn cầu
Amino axit là một loại hợp chất hữu cơ tạp chức. Có thể tác dụng được với cả dung dịch axit và bazơ. Trong đó có Amino axit tác dụng với H2SO4. Hãy cùng CCBook tìm hiểu về Amino axit là gì? Các dạng bài tập và phương pháp giải của Amino axit nhé!

Amino axit là gì?
Trước khi đi vào tìm hiểu Amino axit tác dụng với H2SO4. Các em cần phải nắm chắc được Amino axit là gì? Có các amino axit cần nhớ nào?
Amino axit là một loại hợp chất hữu cơ tạp chức. Bên trong phân tử có chứa đồng thời – NH2 nhóm amino và -COOH nhóm cacbonxyl.
Ví dụ: NH2– C2H4– COOH
Công thức tổng quát của amino axit là: R(NH2)x(COOH)y hoặc CnH2n+2-2k-x-y(NH2)x(COOH)y. Amino axit y có công thức dạng ncxhy(cooh)m.
Tên thay thế của amino axit là gì ?
Chúng ta sẽ sử dụng công thức sau để đọc đúng tên thay thế của một amino axit.
| Axit + Số chỉ vị trí nhóm –NH2 + amino + tên hidrocacbon no tương ứng ở mạch chính + oic |

Axit 2-aminopropanoic.
Tên thường của các amino axit cần nhớ

Cấu tạo phân tử của amino axit
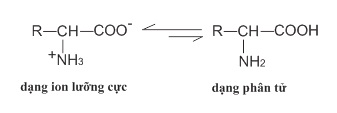
Trên đây, các em đã cùng CCBook tìm hiểu amino axit là gì? Các amino axit nào cần nhớ để áp dụng vào làm bài tập rồi. Giờ CCBook sẽ hướng dẫn phương pháp giải bài tập amino axit tác dụng với H2SO4 và các chất khác.
Amino axit là gì?- Đầy đủ kiến thức từ A-Z để ôn thi THPT QG 2019
Các dạng bài tập amino axit và phương pháp giải
Dạng 1: Amino axit tác dụng với H2SO4 dung dịch axit hoặc bazo
CTTQ: (NH2)xR (COOH)y . Tìm x, y, R?
Amino axit tác dụng với H2SO4 và axit HCL
(NH2)xR (COOH)y + xHCl → (ClNH3)xR (COOH)y
+ x = nHClnaanHClnaa
+ BTKL: maa + mHCl = m muối
Maa + 36,5 x = M muối
Ví dụ 1 Amino axit tác dụng với H2SO4: Amino axit X có công thức H2NCxHy(COOH)2. Cho 0,1 mol X vào 0,2 lít dd H2SO4 0,5M, thu được dd Y. Cho Y phản ứng vừa đủ với dd gồm NaOH 1M và KOH 3M, thu được dd chứa 36,7 gam muối. Phần trăm khối lượng của nitơ trong X là:
A. 9,524%
B. 10,687%
C. 10,526%
D. 11,966%
Lời giải bài tập amino axit tác dụng với H2SO4

Amino axit tác dụng với dd NaOH
(NH2)xR (COOH)y + y NaOH → (NH2)xR (COONa)y + y H2O
1mol → 1mol => mmuối – maa = 22y
naa => mmuối – m aa
naa = mmuoi−maa22.ymmuoi−maa22.y => nCOOH = naa .y = mmuoi−maa22mmuoi−maa22
y =nNaOHnaanNaOHnaa
Maa + 22y = M muối natri
Ví dụ minh họa
Aminoaxit X có dạng H2N-R-COOH (R là gốc hidrocacbon). Cho 0,1 mol X tác dụng hết với HCl thu dung dịch chứa 11,15 gam muối. Tên gọi của X?
A. Phenylalanin
B. alanin
C. Valin
D. Glyxin
Lời giải chi tiết
Ta có phản ứng:
H2N-R-COOH + HCl ClH3N-R-COOH
0,1 mol 0,1 mol
Mmuối = R + 97,5 = 11,15/0,1 = 111,5 => R =14 => R là CH2
=> X : H2N-CH2-COOH
Dạng 2: Amino axit tác dụng với axit, sau đó lấy hh tác dụng với dd bazo và ngược lại
Amino axit HCl→→HCl (A) NaOH→→NaOH (B)
H2N-R-COOH + HCl ClH3N-R-COOH (A)
ClH3N-R-COOH + 2NaOH H2N-R-COONa (B) + NaCl + 2H2O
=> coi hh A gồm ClH3N-R-COOH và HCl không phản ứng với nhau đều phản ứng với NaOH
2. Amino axit NaOH→→NaOH (B) HCl→→HCl (A)
Tương tự như (a) coi hỗn hợp B là ClH3N-R-COOH và NaOH tác dụng với HCl
Ví dụ minh họa
Cho 0,15 mol axit Glutamic vào 175 ml dung dịch HCl 2M thu dung dịch X. Cho NaOH dư vào dung dịch X. Sau khi phản ứng xảy ra hoàn toàn, tính số mol NaOH
A.0,70
B. 0,50
C. 0,65
D. 0,55
Lời giải chi tiết
Ta có:
Coi hỗn hợp phản ứng với NaOH gồm H2N-C3H5-(COOH)2 và HCl
HCl + NaOH →→ NaCl + H2O
0,35mol 0,35 mol
H2N- C3H5-(COOH)2 + 2NaOH →→ H2N-C3H5-(COONa)2 + 2H2O
0,15 0,3 mol
Số mol NaOH = 0,35 + 0,3 = 0,65 mol chọn C

Trên đây, CCBook- Đọc là đỗ đã hướng dẫn các phương pháp giải bài tập amino axit tác dụng với H2SO4. Các em đừng quên lưu lại và thực hành cho thuần thục nhé.
Sách luyện thi "xử gọn" kiến thức Hóa học của cả 3 năm
Hóa học được coi là môn học "khó nhằn" trong năm học cấp 3. Bởi kiến thức nhiều, vô cùng khó nhớ. Đặc biệt, bước vào kì thi THPTQG 2019, các em cảm thấy mệt mỏi hơn nữa. Vì đây là năm đầu tiên thi cả kiến thức 3 lớp. Khối lượng kiến thức nhiều, mà thời gian ôn thi không thay đổi. Khiến các em đã áp lực, còn áp lực nhiều hơn nữa.
Thấu hiểu những khó khăn các em gặp phải. Đơn vị phát hành sách CCBook và nhà xuất bản Đại học Quốc gia Hà Nội, đã xuất bản cuốn sách Đột phá 8+ môn Hóa học kì thi THPTQG.

- Cuốn sách tổng hợp đủ kiến thức 3 lớp 10, 11, 12 trong 1 cuốn sách duy nhất.
- Đủ các dạng bài tập có trong đề thi.
- Có phương pháp giải nhanh, mẹo làm bài, hướng dẫn bấm máy tính casio.
Ngay từ khi ra mắt, cuốn sách đã được đánh giá là sách luyện thi THPT Quốc gia chuẩn nhất năm 2019. Cuốn sách chắc chắn sẽ là "phao cứu điểm" giúp em bứt phá điểm 8+ môn Hóa học trong kì thi sắp tới. Vì vậy, teen 2k1 đừng chần chờ gì nữa mà không sở hữu ngay "bảo bối" thần kì này nhé!
Xem thêm: Axit amino axetic và tất tần tật các dạng toán hay gặp khi thi THPT QG
Thông tin liên hệ với CCBook - Chuyên sách luyện thi
Ngay bây giờ teen 2k1 hãy CMT SĐT dưới bài viết này hoặc nhắn tin cho fanpage CCBook - Đọc là đỗ bằng cách:
Nhắn tin nhanh nhất: http://m.me/ccbook.vn.
Hotline: 024.3399.2266.
Địa chỉ: Số 10 Dương Quảng Hàm - Cầu Giấy - Hà Nội.
Email: [email protected].
Mới! CC Thần tốc luyện đề 2022 giải pháp giúp sĩ tử TĂNG ĐIỂM CHẮC CHẮN TRONG THỜI GIAN NGẮN (12/01/2022)
Đột phá 8+ phiên bản mới nhất có gì khác biệt so với phiên bản cũ? (21/08/2021)
Giới thiệu bộ sách Đột phá 8+ phiên bản mới dành riêng cho 2K4 (03/08/2021)
Đề thi và đáp án đề thi THPT Quốc gia 2021 môn GDCD (08/07/2021)
