-
-
-
Tổng tiền thanh toán:
-

Tổng hợp kiến thức Hóa học lớp 10 trọng tâm nhất
18/05/2021 Đăng bởi: Công ty cổ phần CCGroup toàn cầu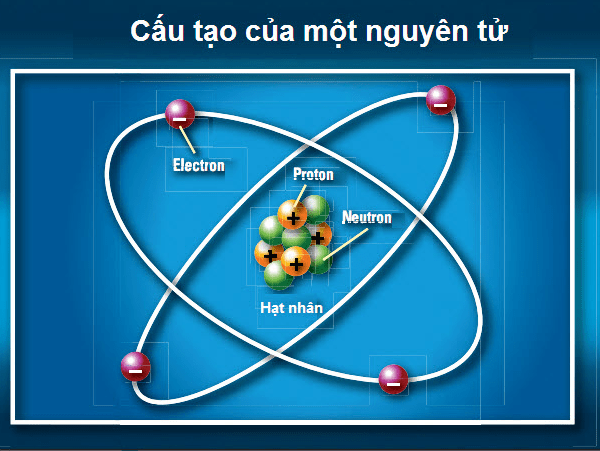
Tổng hợp kiến thức Hóa học lớp 10 sẽ là bước đệm giúp các em tiếp thu kiến thức mới năm 11 tốt hơn. Đặc biệt những em có định hướng chọn môn Hóa làm môn xét tuyển đại học thì sẽ cần chú ý và các kiến thức có liên quan đến đề thi THPT Quốc gia.
Tổng hợp đề thi vào lớp 10 môn Văn năm 2019 tất cả các tỉnh

Các kiến thức Hóa học lớp 10 quan trọng nhất
Tổng hợp kiến thức Hóa học lớp 10
Khi tổng hợp lại kiến thức của cả năm học, trước hết học sinh cần hệ thống lý thuyết. Nắm chắc được tất cả lý thuyết trong tâm, các em mới nên chuyển sang ôn tập các dạng bài. Thời gian trước kì thi THPT Quốc gia tuy còn nhiều, nhưng nếu chúng ta không có sự chuẩn bị ngay từ bây giờ thì đến gần kì thi sẽ không có đủ thời gian.
Trong các đề thi những năm gần đây, kiến thức Hóa học của lớp 10 và 11 luôn xuất hiện. Tỉ lệ câu hỏi rơi vào kiến thức của 2 năm học này lên tới 40-50%. Chính vì thế, các em cần phải thật nghiêm túc trong việc học của mình nếu muốn đạt điểm cao.
Tài liệu mà tự tay các em đã tổng hợp lại sẽ giúp các em dễ nhớ và dễ dàng ôn tập khi cần thiết.
Xem thêm:
- Một số công thức hóa học quan trọng mà teen 2k2 cần ghi nhớ trước thềm năm học 2019
- Đề thi minh họa 2019 và hướng dẫn giải chi tiết
Chương trình Hóa học 10 gồm có 6 nhóm kiến thức quan trọng:
- Nguyên tử – Bảng tuần hoàn các nguyên tố hóa học
- Nhóm Halogen
- Nhóm oxi
- Tốc độ phản ứng và cân bằng hóa học
- Liên kết hóa học- Phản ứng hóa học- Nhận biết
- Bài toán H+, NO3-
Nhìn vào danh sách tổng hợp kiến thức Hóa học lớp 10 trên, các em tự đánh giá xem phần nào mình còn yếu. Nếu yếu thì cần dành nhiều thời gian hơn để củng cố lại. Bài hôm nay sẽ tổng hợp lại kiến thức chương 1 của Hóa học 10 để bạn đọc tham khảo.
Phần tóm tắt lý thuyết Nguyên tử- Bảng tuần hoàn nguyên tố hóa học
Nguyên tử
- Thành phần cấu tạo nguyên tử: Hạt nhân (Proton + Nơtron ) + Vỏ nguyên tử (Electron)
Electron:
me = 9,1094.10-31 kg
qe = -1,602.10-19 C kí hiệu là – eo qui ước bằng 1-
Proton mang điện tích + : Kí hiệu P
m = 1,6726.10-27 kg
q = +1,602.10-19 C kí hiệu eo, qui ước 1+
Nơtron: Không mang điện, khối lượng gần bằng P
- Kích thước & khối lượng nguyên tử
Kích thước : 1A = 10-10 m = 10-8 cm
1nm = 10-9 m; 1nm = 10A. Đơn vị tính A thường dùng nm.
Khối lượng:
Khối lượng của nguyên tử tính bằng U
1u = 1/12 khối lượng 1 nguyên tử đồng vị cacbon-12
1u = 19,9265.10-27 kg/12 = 1,6605.10-27 kg
- Hạt nhân nguyên tử
- Điện tích của hạt nhân:
- Điện tích của Proton: +1. Hạt nhân có Z proton thì điện tích là Z+
- Đơn vị điện tích hạt nhân: Số P= số e.
Ví dụ Na có Z=11+ => Na có số đơn vị điện tích hạt nhân là 11p, 1e.
Số khối:
- Số khối của nguyên tử là tổng số P và N
A= Z+N
Nguyên tử khối= P+N
2. Bảng tuần hoàn nguyên tố hóa học
Bảng tuần hoàn các nguyên tố hóa học
- Nguyên tắc sắp xếp:
- Các nguyên tố hóa học được xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử
- Các nguyên tố có cùng số e trong nguyên tử xếp thành 1 hàng
- Các nguyên tố có cùng số e hóa trị trong nguyên tử xết thành 1 cột
- Cấu tạo của bảng tuần hoàn
Ô số nguyên tố : Số thứ tự của ô bằng với số hiệu của nguyên tử
Chu kỳ: Chu kỳ nhỏ (1,2,3); chu kỳ lớn (4,5,6,7). Là dãy các nguyên tố có cùng lớp e được xết theo chiều điện tích hạt nhân tăng dần. Số thứ tự của các chu kỳ trùng với số lớp e của nguyên tử các nguyên tố trong chu kỳ đó.
Nhóm nguyên tố: s,p,d,f.
Để tải chi tiết bản tổng hợp kiến thức Hóa học lớp 10, các em có thể vào Tài liệu tổng hợp kiến thức Hóa học 10 đầy đủ nhất để tải về.
Tổng hợp kiến thức Hóa học lớp 10- Phần bài tập
Sau khi đã nắm chắc tất cả các phần lý thuyết trong tâm trong sách giáo khoa, các em cần hệ thống dạng bài tập thường gặp.
Các dạng bài tập hay xuất hiện trong bài kiểm tra, bài thi cuối kì và bài thi đại học. Hãy đi từ những dạng bài cơ bản trước.
Các dạng bài Hóa học hay gặp
Chương nguyên tử:
- Xác định tên nguyên tố và viết cầu hình e khi biết tổng số hạt P và N
- Xác định tên nguyên tố và viết cấu hình e nguyên tử khi biết điện tích hạt nhân hoặc ddieejnt ích của lớp vỏ e
- Xác định số khối
- Xác định số lương phân tử loại A2B được tạo thành từ n đồng vị của A, m đồng vị của B.
- Viết cấu hình e của 1 nguyên tử
Trên đây là tổng hợp kiến thức Hóa học lớp 10 phần bài tập chương Nguyên tử về các dạng bài cơ bản nhất. Chia nhỏ các dạng bài, tìm phương pháp giải nhanh là cách giúp các em vừa cùng cố lý thuyết nâng cao khả năng làm bài của mình.
Để biết thêm các phương pháp giải nhanh dạng bài Hóa học lớp 10 các em hãy tham khảo Đột phá 8+ kì thi THPT Quốc gia môn Hóa học. Tại đây có tổng hợp đầy đủ các kiến thức quan trọng liên quan đến đề thi THPT Quốc gia, Không chỉ có các kiến thức lớp 10 mà còn có cả kiến thức lớp 11 và 12.
Lý thuyết và bài tập ví dụ được trình bày song song giúp các em học đến đâu hiểu ngay đến đó.
Hy vọng với bài viết "Hệ thống kiến thức Hóa học lớp 10 trọng tâm nhất" đã nhắc các em nhớ lại lý thuyết cũng như các dạng bài tập cơ bản. Để kết quả học tập ngày càng cải thiện tốt hơn các em hãy chăm chỉ và vận dụng sách Đột phá 8+ kì thi THPT Quốc gia môn Hóa học nhé.
Xem thêm: "Nằm lòng" các công thức Hóa học cơ bản thi THPTQG 2019
Mới! CC Thần tốc luyện đề 2022 giải pháp giúp sĩ tử TĂNG ĐIỂM CHẮC CHẮN TRONG THỜI GIAN NGẮN (12/01/2022)
Đột phá 8+ phiên bản mới nhất có gì khác biệt so với phiên bản cũ? (21/08/2021)
Giới thiệu bộ sách Đột phá 8+ phiên bản mới dành riêng cho 2K4 (03/08/2021)
Đề thi và đáp án đề thi THPT Quốc gia 2021 môn GDCD (08/07/2021)
